Dynamische Lichtstreuung mit dem Malvern Zetasizer Nano-ZS
Der Zetasizer Nano-ZS der Firma Malvern ermöglicht durch Messung der Lichtstreuung die Erfassung von drei unterschiedlichen Partikelcharakteristika in einem flüssigen Medium. Es handelt sich um die Partikelgröße, das Zetapotential und das Molekulargewicht.

Partikelgröße
Die Messung der Partikelgröße basiert bei einem DLS-Messgerät (Dynamische Lichtstreuung) auf der Erfassung der Brownschen Molekularbewegung der Partikel in der Probe. Diese Bewegung kann in Relation zur Partikelgröße gesetzt werden. Praktisch erfolgt eine Messung durch Bestrahlung der Probe mit einem Laser. Auf Grund der Lichtstreuung entsteht auf dem Detektorfenster ein Interferenzmuster aus hellen und dunklen Punkten. Kleine Partikel weisen gegenüber großen Partikeln eine höhere Beweglichkeit auf (Brownsche Molekularbewegung) und verursachen über einen definierten Zeitraum einen schneller fluktuierenden Hell-Dunkel-Zustand auf dem Bildschirm. Anhand der Geschwindigkeit der Fluktuation der Helligkeitspunkte kann auf die Partikelgröße der Teilchen zurückgeschlossen werden. Das Verhältnis zwischen Partikelgröße und Brownscher Molekularbewegung wird durch die Stokes-Einstein-Beziehung beschrieben:

| mit | D | = | Diffusionskonstante |
| k | = | Boltzmannkonstante | |
| T | = | absolute Temperatur | |
| η | = | dynamische Viskosität des Lösemittels | |
| r | = | Partikelradius |
Mit diesem Gerät können Partikelgrößen im Bereich von 0,6 nm bis 6 µm erfasst werden.
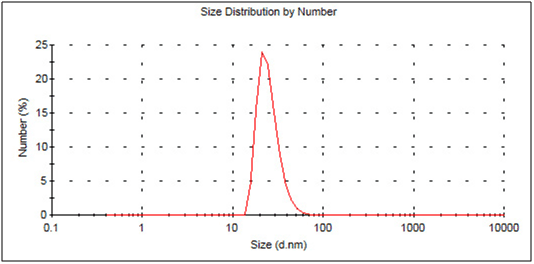
Zetapotential
An der Oberfläche geladener Teilchen entsteht durch Anlagerung einer Schicht von Gegenionen eine sogenannte Sternschicht mit dem Sternpotential. Dort sind die Gegenionen stark an die Oberfläche gebunden. Daran anschließend befindet sich noch eine weitere diffuse Schicht geladener Teilchen, in der sich eine stabile Formation ausbildet. Innerhalb dieser Grenzschicht bewegen sich Ionen bei Bewegung des gesamten Partikels in die gleiche Richtung. Außerhalb der Grenze findet keine gerichtete Bewegung statt, so dass an dieser Grenze eine Scherfläche entsteht. Das Potential an dieser Grenzschicht wird Zetapotential genannt. Die beiden sich ausbildenden Schichten mit unterschiedlicher starker Bindung an das Partikel werden als elektrochemische Doppelschicht bezeichnet.
Die Messung des Zetapotentials erfolgt mit dem Zetasizer Nano indirekt durch Erfassung der elektrophoretischen Mobilität durch eine Laser-Doppler-Geschwindigkeitsmessung in einer Messzelle. Auch hier wird das Licht an Partikeln gestreut und zeigt auf einem Detektor eine Fluktuation der Lichtintensität in Abhängigkeit der Partikelgeschwindigkeit an.
Praktisch erfolgt die Messung durch Anlegen einer definierten Spannung an zwei Elektroden in der Messzelle, die zu unterschiedlichen Geschwindigkeiten der dazwischen liegenden Partikeln führt. Partikel mit höherem Potential weisen eine höhere Geschwindigkeit in diesem Feld auf.
Anschließend kann mit Hilfe der Henry Funktion das Zetapotential berechnet werden.

| mit | UE | = | Elektrophoretische Mobilität |
| ε | = | Dielektrische Konstante | |
| Z | = | Zetapotential | |
| f(Ka) | = | Henry Funktion (Für wässrige Systeme wird ein Wert von 1,5 verwendet. Für kleine Partikel in Medien mit geringer dielektrischer Konstante wird ein Wert von 1 verwendet.) | |
| η | = | Viskosität |
Das Zetapotential ist ein Indikator für die Stabilität von Dispersionen. Aufgrund der gegenseitigen Abstoßung durch die Partikelladung, gelten Dispersionen mit einem Zetapotential oberhalb von 30 mV bzw. unterhalb von -30 mV als stabil und neigen nicht zur Flokkulation.
Zusätzlich existiert noch eine starke Abhängigkeit des Zetapotentials vom pH-Wert. Durch Zugabe von Alkalien bzw. Säuren können die Zetapotentiale je nach Startpunkt vergrößert oder verkleinert werden. Partikel mit negativem Zetapotential können z.B. durch Zugabe von Säure bis zum isoelektrischen Punkt (Zetapotential = 0) und darüber hinaus verändert werden. Der isoelektrische Punkt stellt den instabilsten Punkt einer Dispersion dar.
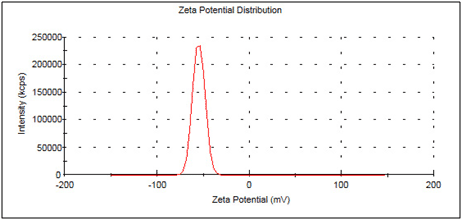
Molekulargewicht
Das Molekulargewicht kann mit dem Zetasizer Nano mit Hilfe von statischer Lichtstreuung (SLS) erfasst werden. Auch hier wird durch Bestrahlung der Probe durch eine Laserlichtquelle eine Lichtstreuung in alle Richtungen erzeugt. Im Gegensatz zur Partikelgrößenmessung und zur Erfassung des Zetapotentials werden nicht die Fluktuationen des gestreuten Lichts erfasst, sondern die über die Zeit gemittelte Intensität der Lichtstreuung. Die Intensität des gestreuten Lichts bei einem definierten Winkel an einem Molekül ist proportional zum Produkt des mittleren Molekülgewichts und der Konzentration der Moleküle. Praktisch wird dazu bei unterschiedlichen Probenkonzentrationen in einer definierten Zeit die Lichtintensität bei einem bestimmten Winkel erfasst. Durch Anwendung der Rayleigh-Gleichung
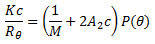
| mit | Rθ | = | Rayleigh-Verhältnis gestreutes Licht zu einfallendem Licht |
| M | = | Molekulargewicht der Probe | |
| A2 | = | zweiter Virialkoeffizient | |
| P(θ) | = | Winkelabhängigkeit der Lichtstreuung | |
| K | = | optische Konstante |
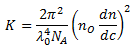
| mit | NA | = | Avogadro-Konstante |
| λ0 | = | Wellenlänge der verwendeten Laserquelle | |
| n0 | = | Brechungsindex des verwendeten Lösemittels | |
| dn/dc | = | Brechungsindexinkrement |
und Auftragung der Intensität des gestreuten Lichts gegen die Konzentration (Debye Plot) kann auf das Molekulargewicht geschlossen werden. Die Extrapolation der Geraden auf den Schnittpunkt mit der Y-Achse (bei X = 0) stellt den reziproken Wert des Molekulargewichts dar.
Mit dem Zetasizer Nano können Molekulargewichte von wenigen hundert g/mol bis hin zu 500.000 g/mol für lineare Polymere und über 20.000.000 g/mol für nahezu kugelförmige Polymere und Proteine erfasst werden.
